|
|||||||
|
|
|
 |
|
|
Strumenti |
|
|
#1481 |
|
Senior Member
Iscritto dal: Apr 2003
Città: Torino
Messaggi: 6818
|
Dovresti preparare una soluzione a base diNaOH (soda caustica) oppure NaHCO3 (bicarbonato di sodio) ed aggiungerla lentamente all'FeCl3. ti precipiterà tutto il ferro come idrossido, rendendo la soluzione neutra o leggermente acida/basica..
Occhio alla soda, quando la sciogli in acqua scalda e la soluzione è pericolosa per pelle ed occhi. Alla soluzione di FeCl3 devi aggiungerla molto lentamente, per evitare produzione di calore/schizzi. Occhio pure se decidi di usare il bicarbonato.. quando versi una soluzione di bicarbonato si verificherà produzione di CO2 e potrebbe formarsi una schiuma che ti invade casa L'idrossido che precipità è qualcosa di molto simile alla ruggine, sostanzialmente innocuo quindi. Comunque, una soluzione diluita di FeCl3 è praticamente innocua, puoi smaltirla senza problemi nello scarico |
|
|

|
|
|
#1482 |
|
Senior Member
Iscritto dal: Dec 2005
Messaggi: 7037
|
Quindi la soluzioni più sicura consisterebbe nell'uso del bicarbonato di sodio.
Interessante. Grazie.
__________________
Distro:Ubuntu LTS, Debian,SL,OpenBSD I love Linux, Bsd and the free software! Fantasia: fotografica  [Icewm]: Thread Ufficiale - light window manager  Benchmark Cpu per sistemi Linux/BSD Benchmark Cpu per sistemi Linux/BSD 
Ultima modifica di AleLinuxBSD : 12-01-2013 alle 09:08. |
|
|

|
|
|
#1483 |
|
Senior Member
Iscritto dal: Mar 2007
Città: Pe-Ch
Messaggi: 19274
|
*edit*
__________________
Ultima modifica di User111 : 11-01-2013 alle 15:22. |
|
|

|
|
|
#1484 |
|
Senior Member
Iscritto dal: Dec 2005
Messaggi: 7037
|
Sciogliendo il bicarbonato di sodio su mezzo bicchiere d'acqua, aspettando che la reazione schiumosa finisca, per poi versalo sopra la soluzione FeCl3, risulterebbe qualcosa di:
- ugualmente efficace - poco efficace - inefficace del tutto ?
__________________
Distro:Ubuntu LTS, Debian,SL,OpenBSD I love Linux, Bsd and the free software! Fantasia: fotografica  [Icewm]: Thread Ufficiale - light window manager  Benchmark Cpu per sistemi Linux/BSD Benchmark Cpu per sistemi Linux/BSD 
|
|
|

|
|
|
#1485 |
|
Senior Member
Iscritto dal: Jun 2003
Città: Padova
Messaggi: 381
|
Una catena corta di Poliacetilene passa dalla forma cis a quella trans o no ?
E se sì con che frequenza ? http://en.wikipedia.org/wiki/Polyacetylene http://it.wikipedia.org/wiki/Poliacetilene Catena corta di esempio CH3-CH-CH=CH-CH=CH-CH3 Detto in altre parole ruota come l' Etano o no ? Passa da questa forma  a questa  Oppure una volta creato è sempre così ? Mi interessa la risposta soprattutto per una catena corta il minimo possibile. Aiuto grazie in anticipo.
__________________
 Lnk ReferendumCostituzionale Ho messo la croce sul NO! per adempiere al mio giuramento militare. Lnk ReferendumCostituzionale Ho messo la croce sul NO! per adempiere al mio giuramento militare.
|
|
|

|
|
|
#1486 |
|
Senior Member
Iscritto dal: Mar 2011
Messaggi: 6309
|
che io ricordi:
attorno ad un doppio legame non è possibile la rotazione => una volta "creato" così rimane ragiona: se fosse possibile "l'intercambiabilità" dal'una all'altra forma, non avrebbe senso sbattersi per dargli 2 nomi diversi claro? |
|
|

|
|
|
#1487 | |
|
Senior Member
Iscritto dal: Mar 2011
Messaggi: 6309
|
Quote:
2-tutta questa reazione "schiumosa" non dovrebbe verificarsi se è solo acqua; 3-si diluisce prima, il bicarbonato in H2O per evitare una reazione troppo intensa =>sviluppo di calore => schizzi; 4-per essere sicuro di neutralizzare tutto il FeCl3, dopo le prime bicchierate di soluzione, aggiungi direttamente bicarbonato fino a saturazione |
|
|
|

|
|
|
#1488 | ||
|
Senior Member
Iscritto dal: Jun 2003
Città: Padova
Messaggi: 381
|
Quote:
un po' diversa, ad esempio il Poliacetilene drogato conduce la corrente elettrica proprio perchè i legami singoli diventano doppi e quelli doppi diventano singoli, quindi un cambiamento avviene, se poi comporti un cambiamento di forma non mi è chiaro. Mi domando se passa da questa forma  a questa  In effetti questa affermazione che segue non è corretta: E' forse troppo riduttiva. Formulo meglio e in maniera semplificata il mio interrogativo: Pensiamo ad una piccola parte della catena di Poliacetilene come se fosse il Butene , è possibile che dell' (nome IUPAC) 1-butene (nome comune) α-butilene 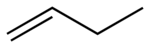 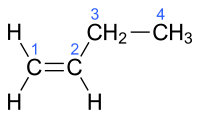  diventi dell' (nome IUPAC) (2Z)-but-2-ene o (cis-but-2-ene) (nome comune) cis-β-butilene  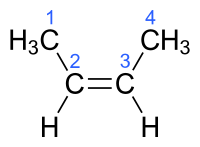  ? ------------------------------------------------------------------------- Quote:
Grazie comunque.
__________________
 Lnk ReferendumCostituzionale Ho messo la croce sul NO! per adempiere al mio giuramento militare. Lnk ReferendumCostituzionale Ho messo la croce sul NO! per adempiere al mio giuramento militare.
Ultima modifica di Bounty_ : 22-01-2013 alle 07:04. |
||
|
|

|
|
|
#1489 | |
|
Senior Member
Iscritto dal: Dec 2005
Messaggi: 7037
|
Quote:
__________________
Distro:Ubuntu LTS, Debian,SL,OpenBSD I love Linux, Bsd and the free software! Fantasia: fotografica  [Icewm]: Thread Ufficiale - light window manager  Benchmark Cpu per sistemi Linux/BSD Benchmark Cpu per sistemi Linux/BSD 
|
|
|
|

|
|
|
#1490 | |
|
Senior Member
Iscritto dal: Mar 2011
Messaggi: 6309
|
Quote:
quella di cui parli è la risonanza, avviene in alcuni casi es. : doppi legami coniugati ciò del tipo -=-=-= ecc. i droganti servono apunto per aumentare questo effetto comunque non vi è trasformazione nella struttura molecolare, ma solo in quella elettronica invece per i due composti da te riportati: non c'è rotazione attorno al doppio legame, non c'è risonanza perchè il doppio legame è uno solo |
|
|
|

|
|
|
#1491 | |
|
Senior Member
Iscritto dal: Apr 2005
Città: Hopp Schwiiz
Messaggi: 2969
|
Quote:
secondo me stai ponendo la domanda in modo sbagliato: come ti é stato gia detto , la conduzione della corrente per drogaggio é dovuto ad delle modificazioni della struttura elettronica o come nel caso specifico per fenomeni di risonanza ( che il drogaggio accentua maggiormente ). Quello che chiedi tu invece , il passaggio da una conformazione CIS ad una TRANS , é invece un problema di stereochimica : se non ricordo male il poliacetilene viene prodotto mediante polimerizzazione Ziegler-Natta e quindi l'ottenimento di uno stereoisomero piuttosto che l'altro dipende fondamentalmente da come avviene l'attacco della macromolecola in accrescimento ( con un carbanione terminale ) sul monomero legato al catalizzatore ( che presenta un carbocatione ). Vanno oltrettutto tenuti in considerazione anche gli effetti dovuti all'ingombro sterico ( sul C positivo ) che orientano la reazione. Comunque sia , se ma macromolecola attacca sempre il carbocatione dalla stessa parte , ottieni un polimero CIS e , ovviamente , TRANS se l'attacco avviene dalla parte opposta del piano. In condizioni normali la struttura del poliacetilene non puo' passare da CIS a TRANS a causa della presenza dei doppi legami nella struttura polimerica . Nel caso invece del PA drogato si ha passaggio di corrente a causa della presenza di "cariche" positive o negative che possono muoversi lungo la catena per azione di un campo elettrico ma cio' non comporta un riarrangiamento della struttura del polimero. Spero di essere stato utile
__________________
Ryzen 5800x, ASUS Crosshair Formula VIII, G.Skill Ripjaws V 4x32Gb 3600, Zotac Trinity 3090, Samsung 1 Tb 980 PRO, Samsung 970 Evo Plus 1 Tb, Icy Box IB-PCI214M2-HSL + Samsung 960 PRO 1 Tb, Full liquid by EK Monoblock+GPU |
|
|
|

|
|
|
#1492 | ||
|
Senior Member
Iscritto dal: Jun 2003
Città: Padova
Messaggi: 381
|
Su quanto sopra ci ritornerò (intanto ringrazio dell'aiuto) avevo in mente anche altri casi.
(tipo chinone che può trasformarsi in fenolo, mi pare di ricordarmi) Ora chiedo, qualcuno sà come si accede, consulta il "Beilstein database" ? Quì http://en.wikipedia.org/wiki/Beilstein_database dicono che sia il più grande database al mondo di chimica organica : Quote:
------------------------------------------------------------------------------------------------------- 27/Febbraio/2013 h20:51 Quì http://guides.lib.usf.edu/beilstein dicono che bisogna collegarsi a: https://www.reaxys.com/reaxys/secured/start.do ma io ottengo sul browser Quote:
Aiuto Grazie.
__________________
 Lnk ReferendumCostituzionale Ho messo la croce sul NO! per adempiere al mio giuramento militare. Lnk ReferendumCostituzionale Ho messo la croce sul NO! per adempiere al mio giuramento militare.
Ultima modifica di Bounty_ : 27-02-2013 alle 19:53. |
||
|
|

|
|
|
#1493 |
|
Senior Member
Iscritto dal: Jan 2006
Città: Pisa
Messaggi: 2417
|
Tutto il vecchio catalogo Beilstein e' stato confluito in Reaxys, che e' una *grossa* banca dati a pagamento (e costa un sacco di quattrini). Per consultarla e' necessario un accesso da un'istituzione che la possieda (c'e' il controllo per IP).
__________________
|
|
|

|
|
|
#1494 |
|
Senior Member
Iscritto dal: Mar 2007
Città: Pe-Ch
Messaggi: 19274
|
secondo voi come si determina l'abbondanza relativa degli elementi chimici?
 spettrometria di massa?
__________________
|
|
|

|
|
|
#1495 |
|
Senior Member
Iscritto dal: Apr 2004
Città: La regione del Triplete
Messaggi: 5726
|
Livelli energetici e principio dell'aufbauf
Perchè un orbitale 4s ha un livello di energia più basso di un 3d, secondo il principio dell'aufbauf?
__________________
Trattative felicemente concluse con domienico120, xbax88 ed engiel, ottimi e seri utenti. |
|
|

|
|
|
#1496 | |
|
Senior Member
Iscritto dal: Mar 2007
Città: Pe-Ch
Messaggi: 19274
|
Quote:
__________________
|
|
|
|

|
|
|
#1497 |
|
Senior Member
Iscritto dal: Jun 2003
Città: Padova
Messaggi: 381
|
Salve ero capitato quì :
http://www.pirika.com/ENG/TCPE/BP-Theory.html ho proseguito quì : http://www.pirika.com/ENG/TCPE/H2U-Joback-H5.html E' un programma che si basa su : http://en.wikipedia.org/wiki/Joback_method Scusate la lacuna ma non capisco cosa voglia dire il > o il < in questo contesto: Ring groups -CH2- >CH- >C< =CH- =C<  Aiuto Grazie
__________________
 Lnk ReferendumCostituzionale Ho messo la croce sul NO! per adempiere al mio giuramento militare. Lnk ReferendumCostituzionale Ho messo la croce sul NO! per adempiere al mio giuramento militare.
|
|
|

|
|
|
#1498 |
|
Senior Member
Iscritto dal: Jan 2006
Città: Pisa
Messaggi: 2417
|
Quando ci mette < o > intende che quel carbonio e' sostituito con due legami singoli, - e' un legame singolo, = e' un legame doppio.
__________________
|
|
|

|
|
|
#1499 |
|
Senior Member
Iscritto dal: Apr 2003
Città: Torino
Messaggi: 6818
|
|
|
|

|
|
|
#1500 | |
|
Senior Member
Iscritto dal: Apr 2003
Città: Torino
Messaggi: 6818
|
Quote:
 I motivi sono da ricercare nello schermaggio agente sugli elettroni negli orbitali di tipo d ( ma pure p ed f) al confronto con gli orbitali s ( che sono più penetranti ed hanno minor momento angolare) e risentono maggiormente dell'interazione elettrostatica con il nucleo. Gli orbitali d risentono maggiormente della repulsione (meno penetranti, maggior momento angolare) dovuta agli altri elettroni dell'atomo e risultano quindi meno legati. |
|
|
|

|

|
| Strumenti | |
|
|
Tutti gli orari sono GMT +1. Ora sono le: 03:00.














_XXL.jpg)





